Approvazione definitiva del vaccino Pfizer? Sui social lo stralcio del documento ufficiale della Fda diventa verità alternativa. Ma scorretta
Il 23 agosto la Food and Drug Administration (Fda), l’ente statunitense che regolamenta i prodotti alimentari e farmaceutici, ha dato l’approvazione definitiva al vaccino anti-Covid di Pfizer-BioNTech per le persone dai 16 anni in su. Finora il farmaco era stato utilizzato grazie a un’autorizzazione d’emergenza, ottenuta l’11 dicembre 2020. Nonostante la lettera di approvazione sia disponibile per tutti sul sito della Fda (qui il link), sui social network si è diffusa la teoria che il vaccino di Pfizer non sia stato veramente approvato. Una bufala, costruita facendo leva un altro documento, ovvero la lettera di autorizzazione all’uso di emergenza riemessa sempre in data 23 agosto. Questo documento, però, non fa altro che specificare come l’autorizzazione di emergenza resti in vigore per determinate categorie, in particolare i bambini dai 12 ai 15 anni (qui il link).

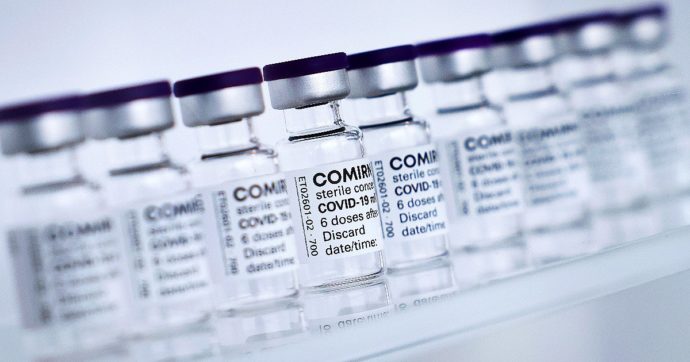
La lettera di approvazione (vedi l’immagine qui sopra) è chiarissima: comunica l’approvazione della biologics license application (Bla), in poche parole l’autorizzazione al commercio del prodotto, che ora potrà essere distribuito col marchio Comirnaty. Nella lettera rivolta a BioNTech si legge: “In base a questa licenza, sei autorizzato a produrre il prodotto, vaccino COVID-19, mRNA” per la prevenzione della malattia Covid-19 “in individui di età pari o superiore a 16 anni“. Quest’ultima specifica è importante: il vaccino Pfizer, infatti, resta disponibile con l’autorizzazione di emergenza per quanto riguarda i bambini dai 12 ai 15 anni. Non solo: la Eua (emergency use authorization) resta in vigore anche per la terza dose a determinate categorie di persone immunodepresse. Inoltre, “continua a coprire l’uso del vaccino Pfizer-BioNTech per ragioni logistiche”, come specifica la stessa Fda. Proprio queste specifiche vengono sottolineate nel secondo documento, denominato “lettera di autorizzazione (riemessa)”.
Nel testo vengono ripercorse le tappe che hanno portato appunto all’approvazione definitiva: infatti si legge che “il 23 agosto 2021, la Fda ha approvato la biologics license application (Bla) presentata da BioNTech Manufacturing GmbH per Comirnaty (vaccino COVID-19, mRNA) […] in individui di 16 anni e più vecchi”. Il documento quindi serve ad autorizzare nuovamente l’uso di emergenza del vaccino Pfizer per quei casi che “non sono inclusi“, così è scritto, nell’approvazione definitiva. Lo si legge ancora poche righe più in basso: “Autorizzo l’uso di Comirnaty (vaccino COVID-19, mRNA) ai sensi di questo Eua (autorizzazione all’uso d’emergenza, ndr) quando utilizzato per fornire un regime a due dosi per individui di età compresa tra 12 e 15 anni, o per fornire una terza dose a individui di età pari o superiore a 12 anni che sono stati sottoposti a trapianto o a cui è stata diagnosticata una condizione che si ritiene abbia un livello equivalente di immunocompromissione”.
Chi vuole sostenere che non ci sia stata nessuna approvazione definitiva, invece, cita solo pagina 13, l’ultima di questo documento. Si legge: “Questo prodotto non è stato approvato o concesso in licenza dalla Fda, ma è stato autorizzato per l’uso in emergenza dalla Fda […] in individui di età pari o superiore a 12 anni”. Peccato che questa condizione si riferisca appunto all’uso del vaccino per le categorie di cui sopra (12-15enni, terza dose per gli immunodepressi). Per le altre vale l’approvazione definitiva. Nello specifico, Fda specifica che l’uso di emergenza continua a valere per tutti solamente “per ragioni logistiche”. Proprio il documento citato impropriamente da chi sta diffondendo la bufala spiega il perché. “Comirnaty è ora concesso in licenza per individui di età pari o superiore a 16 anni”: se fosse ancora necessario, viene ripetuto per l’ennesimo volta che è arrivata l’approvazione definitiva. “Rimane tuttavia – prosegue il testo – una quantità significativa di vaccino Pfizer-BioNTech che è stato prodotto ed etichettato in conformità con questa autorizzazione all’uso di emergenza. Questa autorizzazione rimane quindi in vigore rispetto a quel prodotto per l’indicazione e gli usi precedentemente autorizzati”.
Questo documento, in estrema sintesi, non fa altro che confermare il fatto che il vaccino Pfizer-BioNTech ha ricevuto l’approvazione definitiva e spiega solamente in quali casi valga ancora l’autorizzazione all’uso di emergenza. La stessa Food and Drug Administration nella sua sezione dedicata alle Faq spiega “come è arrivata alla decisione di approvare Comirnaty”. Il disco verde definitivo è basata su dati aggiornati di esperimenti clinici, compresi follow-up di più lunga durata, con la sicurezza e l’efficacia valutati in oltre 40mila persone. “L’analisi aggiornata per determinare l’efficacia per gli individui di età pari o superiore a 16 anni includeva circa 20mila destinatari di Comirnaty e 20mila destinatari di placebo che non avevano evidenza di infezione da Sars-CoV-2 fino a sette giorni dopo la seconda dose. Nel complesso, il vaccino è stato efficace al 91%, con 77 casi di Covid-19 verificatisi nel gruppo vaccinato e 833 casi nel gruppo placebo”, scrive la Fda. La sicurezza invece “è stata valutata in circa 22mila destinatari di Comirnaty e 22mila destinatari di placebo di età pari o superiore a 16 anni. Più della metà dei destinatari del vaccino e del placebo sono stati seguiti per sicurezza per almeno quattro mesi dopo la seconda dose”.

