Covid, Janssen (J&J): “I dati dimostrano che la risposta anticorpale del nostro vaccino è robusta per otto mesi”
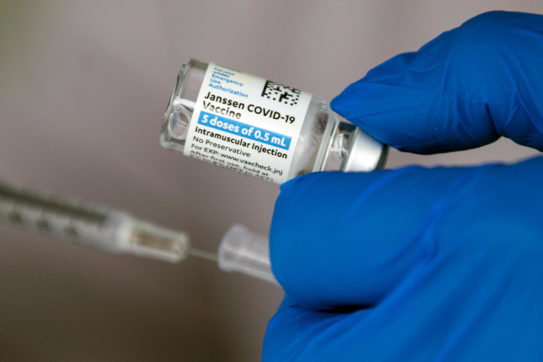
Non ci sta la Janssen (Johnson&Johnson) a passare come la casa farmaceutica il cui vaccino anti Covid – a vettore virale e monodose – sembrerebbe perdere efficacia più velocemente degli altri. “A luglio sono stati pubblicati i dati che dimostrano che le risposte anticorpali generate dal vaccino contro il Covid-19 a dose singola sono rimaste robuste e stabili per otto mesi dopo l’immunizzazione. Uno studio basato su dati del mondo reale registrati fino a oggi negli Usa pubblicato a settembre ha dimostrato un’efficacia stabile del vaccino del 79% per le infezioni e dell’81% per i ricoveri. Non ci sono state evidenze di efficacia ridotta, compreso quando la variante Delta è diventata dominante”. Nella nota la divisione vaccini di J&J sottolinea che il richiamo – all’inizio non previsto – a 6 mesi ha dato un aumento degli anticorpi di 12 volte. Sulla durata dell’efficacia ieri si era espresso anche il professor Andrea Crisanti criticando la casa farmaceutica .

Mentre è stato il professor Franco Locatelli, coordinatore Comitato tecnico scientifico, a ipotizzare un richiamo con un vaccino a Rna messaggero per chi ha ricevuto il monodose svelando che la Food and drug administration ha in corso un processo di revisione. Oggi è arrivato l’annuncio del sottosegretario alla Salute, Pierpaolo Sileri, che la terza dose di vaccino sarà per tutti e che verrà data una priorità a quelli immunizzati con il composto della Janssen. Intanto all’esame della Commissione tecnico consultiva dell’Agenzia italiana per il farmaco nella riunione del 28 ottobre ci sarà proprio l’ipotesi di un nuova dose per coloro che hanno ricevuto il vaccino di Johnson&Johnson. A chiedere un parere all’ente regolatorio italiano è stato proprio il ministero della Salute. Tra le ipotesi anche la possibilità che per la nuova inoculazione venga utilizzato un vaccino a mRna, Pfizer o Moderna. Non solo: secondo fonti qualificate, la somministrazione non deve essere considerata come un richiamo, poiché l’immunizzante J&J è monodose e per una nuova somministrazione non sarebbe necessario aspettare che sia trascorso il periodo di sei mesi.
A dare il via libera al booster è stata proprio la Fda il 20 ottobre scorso raccomandandolo a tutte le persone dai 18 anni in su che hanno ricevuto la prima dose almeno due mesi fa. La stessa Fda ha autorizzato contestualmente l’uso per il richiamo di un vaccino diverso da quello ricevuto inizialmente per tutti e tre i vaccini autorizzati in America (Moderna, Johnson&Johnson e Pfizer), strategia denominata ‘mix and match’. Ora, in attesa che anche l’Agenzia del farmaco europea (Ema) si pronunci sull’argomento, l’Aifa potrebbe dare il suo parere già nei prossimi giorni. Bisogna infine ricordare che in Italia questo vaccino – come l’altro a vettore virale Astrazeneca – è consigliato agli over 60.

