Vaccino Johnson&Johnson, riunione ministero della Salute-Aifa dopo lo stop Usa. Magrini (Aifa): “Valutiamo a breve se darlo agli over 60”

Nel giorno dell’arrivo delle prime 184mila dosi del vaccino Janssen di Johnson&Johnson, lo stop annunciato dagli Usa mette in allerta il ministero della Salute. Alle 16.30 è stata convocata una riunione tecnica – alla quale hanno preso parte anche l’Agenzia italiana del farmaco, rappresentanti dell’Istituto Superiore di Sanità e del Comitato tecnico scientifico – sulla mossa decisa dalla Fda e dai Cdc di sospendere il farmaco anti-Covid dopo 6 casi di trombosi in donne giovani negli Stati Uniti.
Al termine del vertice, il ministro della Salute Roberto Speranza ha spiegato: “Abbiamo fatto una riunione con Aifa e scienziati, siamo in contatto con Ema e valuteremo nei prossimi giorni appena a Ema e Usa daranno informazioni definitive quale sarà la strada migliore, ma penso che anche questo vaccino dovrà essere usato, perché è importante”. Il ministro della Salute ha quindi ribadito come “la scelta statunitense è una scelta precauzionale” e la “scelta di Johnson &Johnson di non immettere immediatamente in commercio il vaccino in Europa è anch’essa una scelta di natura precauzionale”. L’auspicio – ha sostenuto Speranza a Porta a Porta – è di “poter al più presto sciogliere questi nodi e usare anche questo vaccino che sarebbe il quarto, e che a noi serve particolarmente”.
“Valuteremo se dare il vaccino Janssen contro Covid-19 agli over 60, e lo faremo non appena si potrà riprendere la campagna vaccinale” con questo vaccino, “nel giro di 2-3 giorni, forse anche meno. Se poi si potrà aprire alla somministrazione dal medico di famiglia, in farmacia o nei punti di libero accesso che aumenteranno, lo vedremo”, afferma il direttore generale dell’Agenzia italiana del farmaco, Nicola Magrini. “Guardiamo a quello che decideranno gli organismi americani – spiega – dopo la segnalazione di sei casi su 7 milioni vaccinati, un rischio di 1 per milione, rarissimo. Anche in questo caso si tratta di donne giovani, tra 18 e 48 anni, potrebbe essere un meccanismo simile a quello del vaccino AstraZeneca”. Basta un caso per milione per bloccare un farmaco? “No – risponde Magrini – sono fiducioso che individuando le categorie a maggior rischio di ammalarsi di Covid grave, i benefici” della vaccinazione “sono assolutamente non confrontabili con questi rischi molto rari”.
Nel pomeriggio anche Ema ha comunicato che sta “indagando sui casi” di trombosi rare segnalate dopo la vaccinazione anti-Covid “per decidere se sia necessaria un’azione” dal punto di vista “regolatorio”. L’Agenzia europea del farmaco ha avviato la revisione sui segnali di sicurezza riguardanti questo prodotto scudo, come annunciato nei giorni scorsi facendo il punto su quanto emerso dalla riunione del Comitato di farmacovigilanza Prac dell’Agenzia, e ha precisato che al momento “non è chiaro se c’è un link causale fra il vaccino e i coaguli” osservati.
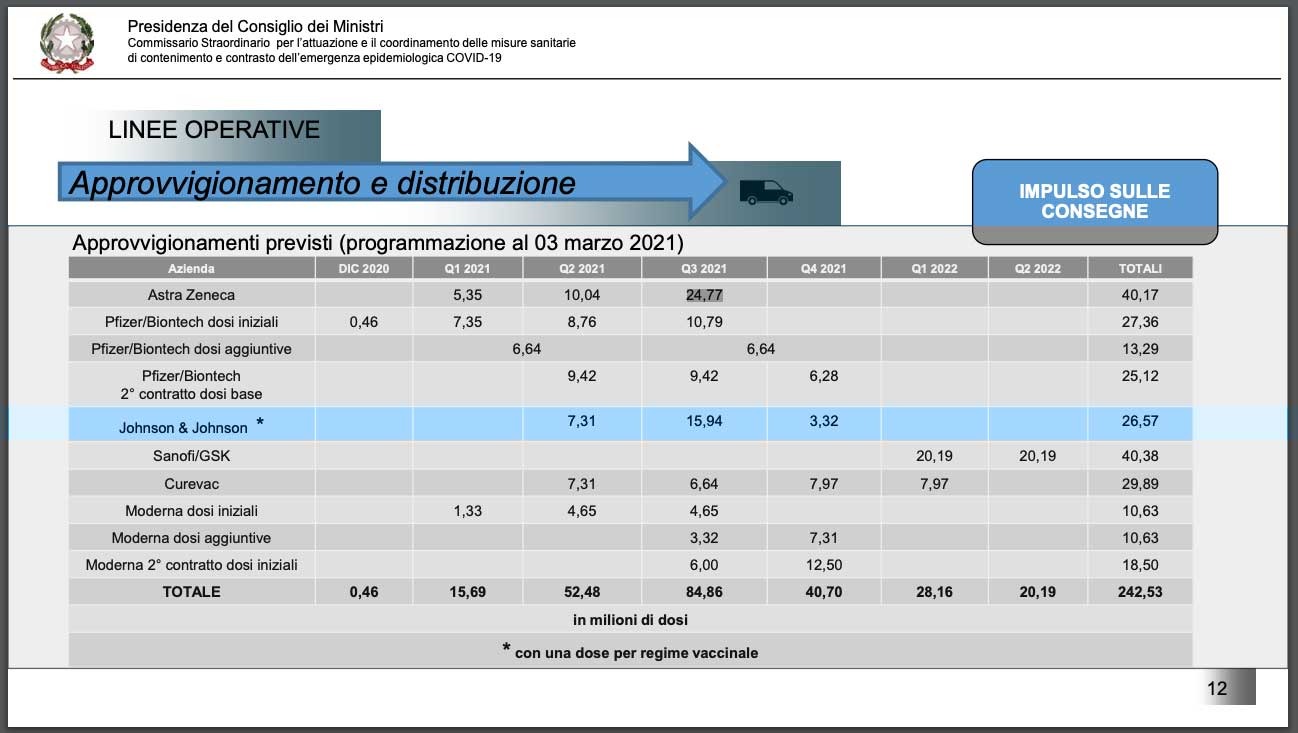
Nel piano vaccinale nazionale, presentato esattamente un mese fa dal commissario all’emergenza Francesco Paolo Figliuolo, è previsto l’arrivo di 26,57 milioni di dosi di Johnson&Johnson in Italia entro la fine di quest’anno. In dettaglio, come indicato nelle tabelle, 7,31 milioni di dosi nel secondo trimestre, quello appena iniziato. Altri 15,94 milioni sono previste nel terzo, mentre 3,32 saranno consegnate negli ultimi tre mesi del 2021. Si tratta di oltre il 10 per cento del totale di dosi previste – compresi Sanofi/Gsk e Curevac – nel corso dell’anno e nei primi due quadrimestri del 2022, tra l’altro di un vaccino monodose.
Poche ore prima della notizia comunicata dalle autorità sanitarie Usa, Figliuolo aveva avvisato che nel pomeriggio sarebbero arrivate 184mila dosi nell’hub della Difesa di Pratica di Mare. Le dosi con ogni probabilità resteranno nel centro fino a quando non verrà presa una decisione definitiva, tenendo conto che Johnson&Johnson ha comunicato di aver cancellato tutte le consegne in Europa in attesa di chiarire ogni aspetto. Si tratta del primo lotto del vaccino che, insieme, alle circa 175mila dosi di Vaxzevria vanno a comporre in parte dei 4,2 milioni di dosi in arrivo tra il 15 e il 22 aprile e che dovrebbero contribuire “in modo significativo”, specificava il commissario al raggiungimento del target della campagna vaccinale.
I Centers for Disease Control and Prevention e la Food and Drug Administration americani hanno raccomandato una “pausa” come misura di “estrema precauzione” in attesa che domani venga convocato l’Advisory Committee on Immunization Practices, comitato del Cdc per le vaccinazioni, “per analizzare” i casi di trombosi che si sono verificati per almeno sei donne vaccinate. L’Agenzia americana del farmaco poi analizzerà questi “dati e indagherà questi casi”, si legge in una dichiarazione diffusa oggi dalle agenzie federali. Dubbi di fronte ai quali la multinazionale ha risposto specificando che “al momento non è stato dimostrato nessun nesso causale chiaro fra questi eventi rari” e il vaccino Janssen contro il coronavirus.