Il premio Nobel alla chimica verde ed efficiente: ecco cos’è l’organocatalisi asimmetrica

Dopo la bellissima notizia del Nobel a Giorgio Parisi, arriva il premio più ambito anche a Benjamin List e a David Mac Millan per la Chimica.
Grandi emozioni anche personali perché si tratta proprio del campo di ricerca nel quale ho lavorato nel 2003 in Danimarca e che ho portato (insieme a tanti altri) a Roma nel 2005 quando sono ritornato in Italia come ricercatore. Tra l’altro, ironicamente, List (che conosco bene) ha fatto la sua scoperta proprio in quel posto incredibile per la scienza che è Scripps Research Institute, a San Diego, a poche decine di metri dove ho lavorato e vissuto anche io per oltre due anni.
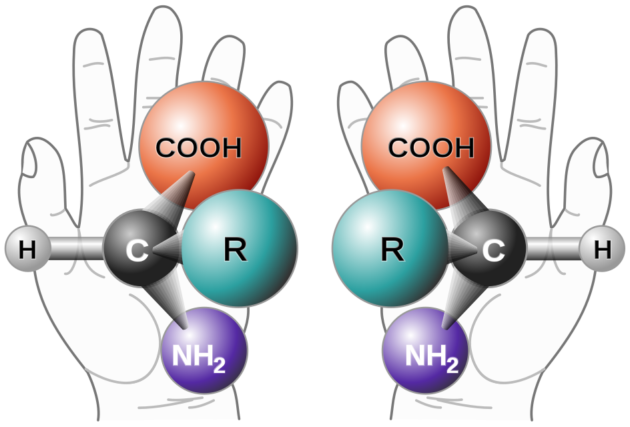
La storia dietro a questo Nobel è affascinate e anche un po’ controversa. Buona parte delle molecole sono chirali cioè sono oggetti con le stesse proprietà delle nostre mani: ne esistono due versioni che sono l’uno l’immagine riflessa allo specchio dell’altra. Ovviamente, fare una sola “mano” è difficilissimo, di fatto impossibile fino pochi decenni fa. Chi ha provato a dire “ma sì, mettiamo le due mani insieme, tanto che vuoi che succeda” si è scontrato con una dura realtà: il nostro corpo riconosce le molecole chirali.
C’era un farmaco, la talidomide, che era venduto appunto come “due mani” insieme. Una “mano” era un antiemetico, cioè preveniva i disturbi della gravidanza come il vomito, ma l’altra “mano” era teratogena, cioè provocava delle malformazioni gravissime come la focomelia (mancanza di arti). Questo caso esplose in Germania e poi nel resto d’Europa negli anni 60 e il farmaco fu ritirato da mercato dopo aver causato tantissima sofferenza a tantissime famiglie.
È quindi nata l’esigenza di preparare le molecole tramite “catalizzatori chirali” ovvero sostanze che accelerano la reazione e producono una sola “mano”. Anche qui però sono sorti dei problemi: i catalizzatori chirali maggiormente impiegati fino al 2000 contenevano metalli pesanti, costosissimi, potenzialmente tossici, difficili da smaltire e che avevano bisogno di condizioni molto particolari, cioè ad esempio l’assenza rigorosa di aria e acqua.
Che cosa succede nell’anno 2000? Sia List che Macmillan scoprono che queste reazioni difficilissime potevano anche essere condotte tramite catalizzatori organici, cioè sostanze che non avevano bisogno dei metalli di transizione, e che addirittura un po’ di acqua non solo faceva funzionare lo stesso la reazione, ma era in alcuni casi persino di aiuto. Tra l’altro gli organocatalizzatori sono sostanze non tossiche che si potevano persino mangiare: non solo la prolina usata da List ma anche la chinina (la sostanza naturale antimalarica) e derivati che ho usato io e tanti altri, come il mio capo danese, Karl Anker Jorgensen, che a detta di molti avrebbe potuto meritare anche lui il Nobel.
A questo punto è nata una nuova branca della chimica, che era anche una filosofia di come condurre la sintesi organica. C’erano quelli che controllavano rigorosamente tutte la condizioni di reazione evitando che anche la più piccola traccia di acqua o aria entrasse e facevano catalisi metallica e gli altri, “gli zozzoni”, cioè quelli come me, che invece cercavano di sviluppare nuove reazioni ove anche un po’ di acqua o aria non cambiasse granché.
Con gli anni, l’industria chimica ha trovato sempre più interessante quello che facevano gli “zozzoni”, perché magari in laboratorio riesci pure a escludere acqua e aria da un piccolo pallone di reazione, ma quando poi lo devi fare in un reattore da 100 kg diventa tutto più difficile se non impossibile. Per non parlare del fatto che in alcune reazioni chimiche industriali il 60% dei costi è legato all’uso e smaltimento del catalizzatore metallico. Senza usare metalli di transizione diventava tutto più semplice e ci si muoveva finalmente verso una chimica verde ed ecosostenibile!
In realtà, in questo campo non c’era nulla di totalmente nuovo. Cercando nella letteratura si è visto che gli organocatalizzatori erano stati usati addirittura prima del ‘900 e che quello usato da List nel 2000 era stato impiegato negli anni 70 da due gruppi di ricerca per sviluppare la reazione nota come reazione di Hajos–Parrish–Eder–Sauer–Wiechert, dal nome degli scopritori.
Dal 2000 in poi l’organocatalisi asimmetrica è esplosa come campo di ricerca, passando nel giro di pochissimo a migliaia di pubblicazioni all’anno e moltissimi gruppi di ricerca che se ne sono occupati (tra cui il mio a Roma Sapienza). Questo Nobel probabilmente sarebbe potuto arrivare molti anni fa anche se c’era un problema: con così tante persone che lavoravano in questo campo (il Nobel si può dare a massimo tre persone) era difficile scegliere a chi darlo, perché sarebbero dovuti essere riconosciuti anche coloro che negli anni 70 avevano iniziato questo campo di ricerca, poi dimenticato per quasi trent’anni.
Per non parlare anche dell’ex capo di List all’epoca, Carlos Barbas III (deceduto per un tumore nel 2014), con il quale List scrisse il suo primo articolo sull’organocatalisi e con il quale si separò non rimanendo affatto in buoni rapporti. In questa area c’è stata anche una competizione serrata, con reazioni sviluppate nella versione “organocatalitica” scoperte a distanza di pochi giorni da gruppi di ricerca diversi, tanto che sono sorte anche delle discussioni se le idee fossero state effettivamente “contemporanee” o addirittura “rubate” tra i vari ricercatori.
In ogni caso, a Macmillan e List va sicuramente il merito di aver finalmente fatto riscoprire qualcosa che era lì, che tutti i “cacciatori” di nuove reazioni potevano usare in modo semplice, ma di cui nessuno prima di loro aveva intuito l’incredibile potenziale di cambiare il mondo della chimica e anche il nostro in meglio.



