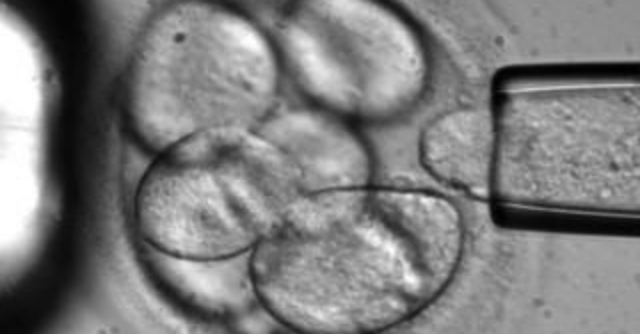
Ottenere cellule staminali embrionali senza distruggere l’embrione e farle crescere in maniera rapida. Descritta sulla rivista su Nature Communications, la tecnica è stata messa a punto dal gruppo di ricerca internazionale guidato dall’istituto svedese Karolinska e permette di prelevare una sola cellula da un embrione di otto cellule senza comprometterne lo sviluppo e di farla moltiplicare in modo consistente in tempi ‘ragionevoli’.
Recenti tecniche, simili a quelle utilizzate anche per le diagnosi genetiche preimpianto, permettono da qualche tempo di isolare una singola cellula dall’embrione giunto allo stadio di otto cellule. Quest’ultimo può essere poi ricongelato e impiantato nell’utero senza pregiudicare lo sviluppo del bambino. Il limite per l’utilizzo di queste staminali embrionali è però nel fatto che la tecnica permette di isolare una sola cellula.
Attualmente le cellule staminali embrionali umane sono ottenute utilizzando il surplus di embrioni creati in vitro che non vengono impiegati per tentare di ottenere una gravidanza. Gli embrioni non sopravvivono alla procedura necessaria all’ottenimento delle staminali. La normativa svedese è fra quelle più permissive: il gruppo di scienziati ha infatti potuto prima di tutto generare cellule da embrioni in eccesso, dopo aver ottenuto il permesso delle persone che avevano donato ovuli e spermatozoi per la Fiv. Ma ha poi sviluppato un metodo che permette di utilizzare una singola cellula di un embrione composto da 8 cellule, e di congelarlo nuovamente. Dopodichè, in teoria, anche utilizzarlo per il trasferimento in utero.
“Sappiamo che un embrione può sopravvivere dopo la rimozione di una singola cellula staminale. E questo fa una grande differenza a livello etico” dice il ricercatore Karl Tryggvason. La cellula viene successivamente coltivata su un ‘letto’ composto da una proteina umana chiamata laminina Ln-521, normalmente associata con le cellule staminali pluripotenti dell’embrione. Ciò consente alla cellula staminale di duplicarsi e di moltiplicarsi senza essere contaminata. In precedenza, invece, la coltivazione di staminali avveniva con proteine animali o cellule umane, cosa che contaminava le staminali. Ora, “possiamo coltivare le staminali in un ambiente chimicamente definito e di qualità clinica. Ciò significa che è possibile produrre cellule staminali embrionali su larga scala, con la precisione richiesta per la produzione farmaceutica – assicura Tryggvason -Grazie a questa tecnologia la fornitura di staminali embrionali umane non sarà più un problema. Sarà possibile creare una banca dove le cellule staminali possono essere abbinate per tipo di tessuto, per evitare ad esempio il rigetto nei trapianti”. Ma le strade terapeutiche percorribili sono le più numerose: dal diabete al Parkinson.
“Il lavoro fatto dai ricercatori svedesi supera questa difficoltà”, ha spiegato il genetista Edoardo Boncinelli, dell’università Vita e Salute di Milano. “Una volta ottenuta una singola cellula, infatti, ci vuole molto tempo, troppo, prima di averne un numero sufficiente per poterle utilizzare. Il nuovo lavoro – prosegue l’esperto – ha sviluppato una sorta di ‘letto’ che accelera la crescita delle cellule e permette alla singola cellula di moltiplicarsi in tempo ragionevole”.
È quindi una tecnica che potrebbe aprire definitivamente la strada all’uso terapeutico delle staminali embrionali embrionali. “A prescindere dal tipo di cellule usate – ha aggiunto Boncinelli – si tratta di un grosso cambiamento in quanto rende più rapido lo sviluppo cellulare ed è stato già verificato sulle cellule umane”. Il successo viene inoltre considerato un ulteriore passo in avanti per il superamento delle limitazioni etiche imposto all’uso delle staminali embrionali “anche se – ha spiegato il genetista – gran parte dei problemi sono stati superati con la produzione delle Ips (Staminali Pluripotenti Indotte) create in vitro. Bisogna sempre ricordarsi che avere le cellule necessarie è solo il punto di partenza non l’arrivo, le cellule vanno infatti ‘educate’ e per riuscire in questo ci vorrà, purtroppo, ancora qualche anno”.
Articolo Precedente
Stephen Hawking e i buchi neri: “Non esistono”. Lo studio su Nature

Articolo Successivo
Otto italiani tra i migliori 400 scienziati al mondo, sei lavorano in Italia